据悉,在今年即将召开的ESMO上,DS-8201与T-DM1头对头的DESTINY-Breast03研究成果将以“最新突破摘要”(LBA,Late-breakingAbstract)形式重磅亮相,这一数据被认为是本次大会最重要、最具轰动性的研究成果。
我国HER2ADC药物的竞争趋于激烈,继T-DM1获批上市后,6月9日,荣昌生物的注射用维迪西妥单抗(RC48)获NMPA批准上市,用于治疗至少接受过2种系统化疗的HER2过表达局部晚期或转移性胃癌患者。除了荣昌生物外,浙江医药、科伦药业、嘉和生物、复星医药等亦深耕于此,未来,HER2ADC竞争格局如何,本文将一探究竟。
(一)T-DM1:国内首个上市的ADC药物
Kadcyla(恩美曲妥珠单抗,T-DM1)是一款HER2ADC药物,于2013年获FDA批准上市,先后获批HER2阳性转移性乳腺癌和接受新辅助治疗后残存病灶的HER2阳性早期乳腺癌的辅助治疗。2020年1月,T-DM1获NMPA批准上市,适应症为接受紫杉烷类联合曲妥珠单抗为基础的新辅助治疗后,仍残存侵袭性病灶的、HER2阳性早期乳腺癌患者的辅助治疗。
在结构的设计上,T-DM1采用曲妥珠单抗,细胞毒药物采用了微管蛋白抑制剂DM1,连接子采用MCCLinker。T-DM1作为早期的ADC药物,其结构设计存在不足,在payload的选择上,DM1毒性有限,不及同为微管蛋白抑制剂的MMAE和MMAF,纵观上市的ADC药物,仅T-DM1采取了DM1作为Payload;此外,由于采用不可裂解的linker,尽管稳定性提升,但不具有旁观者效应(BystanderEffect)。
从作用机制上,T-DM1可与细胞膜表面HER2受体的第Ⅳ亚区结合,内吞后并经溶酶体降解后,在细胞质中释放细胞毒素DM1,破坏细胞的微管蛋白,导致细胞周期阻滞和细胞凋亡。此外,T-DM1经细胞膜内吞后,进入胞内体,部分T-DM1与FcRn结合,经过FcRn介导的再循环被排出膜外,提升药物半衰期。
上市以来,凭借乳腺癌广泛的患者群体和独特的治疗机制,T-DM1全球销售额持续攀升,2020年全球销售额17.45亿瑞士法郎,接近20亿美元,同比增长25%。但在国内市场,T-DM1的销售额难言乐观,根据wind医药库,T-DM1在2020年样本医院销售额仅1665万元,一方面,T-DM1售价较高,即使考虑赠药计划,年治疗费用依然高达26万元;另一方面,适应症较窄且偏,适应症中新辅助化疗限制了患者数量。
(二)维迪西妥单抗:首个上市的国产ADC药物
维迪西妥单抗(RC48)是荣昌生物自主研发的HER2ADC药物,2021年6月9日,维迪西妥单抗获NMPA批准上市,适应症为至少接受过2种系统化疗的HER2过表达局部晚期或转移性胃癌患者。8月26日,CDE官网公示,维迪西妥单抗的新适应症上市申请拟纳入优先审评,用于既往接受过系统化疗且HER2表达为免疫组化检查结果为2+或3+的局部晚期或转移性尿路上皮癌(UC)患者。这标志着维迪西妥单抗有望加速迎来第二个适应症的获批。
从结构上分析,维迪西妥单抗的mAb采用Disitamab,EC50值为6.4pM,较曲妥珠单抗亲和力更强,临床达标剂量更低;Payload采用MMAE,毒性较高,可更好地阻断微管蛋白聚合;采用可裂解linker,可通过旁观者效应实现相邻肿瘤细胞的杀伤。
T-DM1的胃癌适应症已经折戟,维迪西妥单抗为晚期胃癌患者提供新的治疗手段。根据维迪西妥单抗胃癌地Ⅱ期临床研究,维迪西妥单抗三线治疗胃癌ORR达24.4%,中位PFS为4.1个月,中位OS为7.9个月。此外,针对经过二线及以上系统化疗的尿路上皮癌患者,维迪西妥单抗治疗显示出良好的疗效和生存获益,ORR达50%,OS达14.2个月,mPFS达5.1个月。
(三)DS-8201:亮眼数据技惊四座
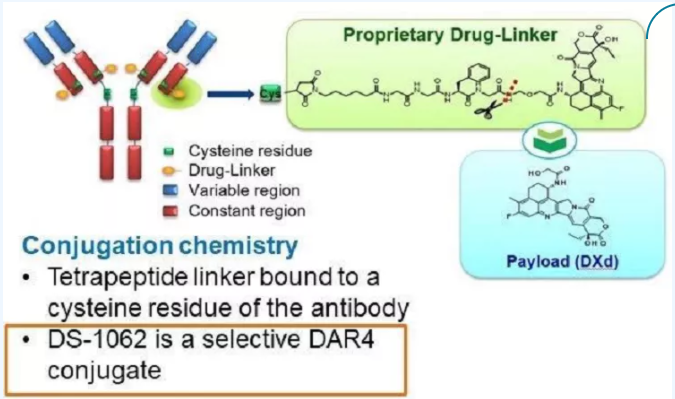
Enhertu(DS-8201)是HER2ADC领域的杰作,由第一三共和阿斯利康联合研发。DS-8201创造了许多奇迹,可谓凭借一己之力改变了ADC领域许多旧观念。最值得一提的是,DS-8201的DAR高达8,即每个抗体分子偶联8个细胞毒药物,这打破了DAR应控制在2-4的传统设计理念。高DAR搭配中等毒性Payload的组合,不仅可以更好发挥抗肿瘤作用,而且脱靶毒性有望降低。
DNA拓扑异构酶抑制剂的选择兼顾安全性和疗效。在payload的选择上,DS-8201采用了DNA拓扑异构酶抑制剂DXd,DXd活性是伊立替康的10倍,与传统微管蛋白抑制剂相比,DNA拓扑异构酶抑制剂优势较多,包括毒性较小,半衰期较短,不易在体内发生蓄积;靶标数量较少,在ADC药物携带相同数量弹头进入细胞的情况下,DNA抑制剂能发挥更好的杀伤作用等。
2019年,DS-8201获FDA批准HER2阳性乳腺癌适应症。实验数据表明,在184例接受推荐剂量的患者中,IRC评估的ORR达60.9%,其中,CR达6%,PR达54.9%,DoR达14.8个月。安全性方面,DS-8201存在中性粒细胞计数下降、贫血、间质性肺炎等AE。总的来说,DS-8201治疗HER2阳性乳腺癌的数据显著优于T-DM1,但间质性肺炎的不良事件在临床使用时值得关注。
2020年,DS-8201再次斩获HER2阳性胃癌适应症,且数据极其亮眼。DESTINY-Gastric01试验显示,DS-8201三线治疗HER2阳性胃癌ORR达40.5%,CR达7.9%,PR达11.3,DoR达11.3个月。凭借这一数据,DS-8201从强者之林脱颖而出,至今尚无上市药物足以与之匹敌,当然,间质性肺炎适应症同样值得警惕。
(四)ARX788:非天然氨基定点偶联技术
ARX788国内开发及商业化权益归属浙江医药子公司新码生物,引自美国ADC药物龙头企业AMBRX。ARX788由曲妥珠单抗与AS269偶联而成,AS269属于Auristatins类毒素,毒性较强。5月18日,ARX788乳腺癌适应症纳入突破性治疗品种,8月10日,ARX788胃癌Ⅱ/Ⅲ期临床试验完成首例入组。
ARX788最核心的技术在于非天然氨基酸定点偶联技术,可生成DAR为2的ADC药物,提升药物的均一性。定点偶联是相对于随机偶联的概念,由于每个抗体均拥有数个或更多的氨基酸位点,因此毒素药物的连接难以控制,DAR的提高削弱了药物均一性,定点偶联的设计通常引入两个特殊氨基酸位点,更有效地控制抗体与毒素药物的连接。
Ambrx非天然氨基酸技术路线分为三步:第一步在体外合成符合成药需求的天然氨基酸,第二步在合成酶的作用下,天然氨基酸与特殊tRNA连接,运送到核糖体中,第三步tRNA识别特殊密码子,精确将天然氨基酸插入到多肽链的特定部位。
(五)A166:赖氨酸定点偶联技术
A166由科伦药业控股子公司科伦博泰研发,是第三代靶向HER2的抗体偶联药物,通过蛋白酶可裂解Linker将新型毒素分子(Duo-5,微管蛋白抑制剂)定点偶联至HER2抗体(曲妥珠单抗)。
在2021年ASCO上,科伦药业公布A166地Ⅰ期临床研究结果,有效剂量4.8和6.0mg/kg下,36例可评估疗效的HER2阳性乳腺癌患者的ORR分别为59.1%(13/22)和71.4(10/14);4例可评估疗效的HER2低表达乳腺癌患者结果为1例PR,2例SD和1例PD。中位PFS未达到,4.8mg/kg剂量组中1例患者接受A166治疗已经超过19个月。安全性方面,A166整体良好可控,但存在眼部不良事件。对于眼毒性,经对症治疗后,均可恢复。
(六)总结
受全球创新浪潮的冲击和ADC药物的更新迭代,HER2ADC已成为国内ADC领域竞争最激烈的领域之一,荣昌生物、浙江医药、科伦药业、嘉和生物、复星医药等均在此布局。除了HER2ADC外,百济神州的ZW49是一款HER2×HER2ADC,可同时结合HER2的两个非重叠表位,有望提升药物的靶向性。但HER2ADC药物的研发并非一帆风顺,百奥泰的BAT8001已经折戟,未来,布局HER2ADC的相关企业一方面需要与时间赛跑,加速研发抢先上市;另一方面采取差异化路径,多适应症布局,在乳腺癌、胃癌、尿路上皮癌等适应症上多点突破。