11月29日,贝达药业收到国家药监局(NMPA)核准签发的《药品注册证书》(药品批准文号:国药准字S20210047),贝伐珠单抗注射液(MIL60,商品名:贝安汀®)正式获批上市,获批的适应症为转移性结直肠癌和晚期、转移性或复发性非小细胞肺癌。
肺癌是中国死亡率和发病率均排名第一的恶性肿瘤疾病,其中非小细胞肺癌(NSCLC)约占肺癌的80%-85%。而在中国常见新发癌症中,结直肠癌的总体发病率已升至第三位,并居常见癌症死亡原因的第五位。
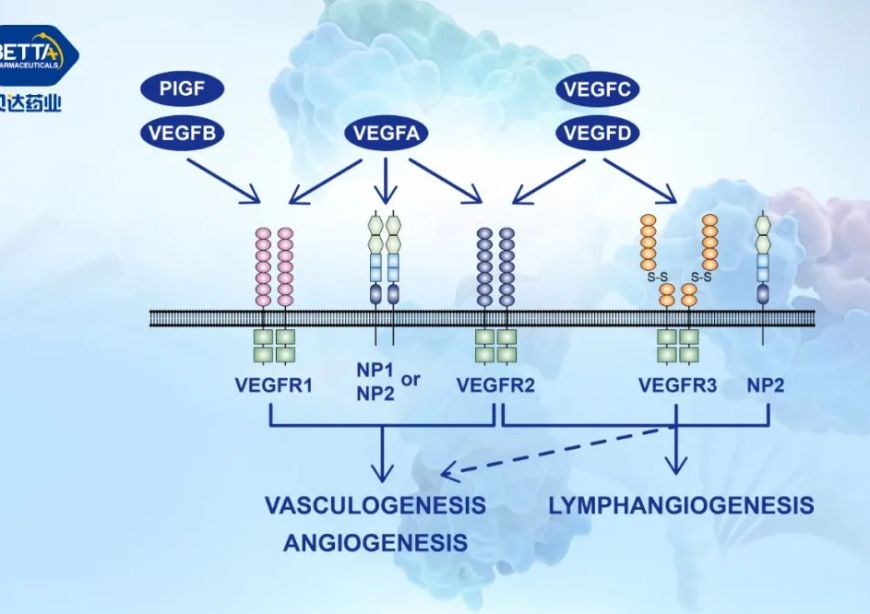
贝伐珠单抗是一种重组的人源化单克隆抗体,可以选择性地与人血管内皮生长因子(VEGF)结合并阻断其生物活性,减少肿瘤的血管形成,从而抑制肿瘤的生长。贝伐珠单抗原研药安维汀®于2015年7月9日获NMPA批准,在与卡铂和紫杉醇联合应用时,可作为一线治疗用于不可切除的晚期、转移性或复发性非鳞状NSCLC患者。
2017年2月,贝达药业与北京天广实生物技术股份有限公司就贝伐珠单抗注射液项目达成合作,受托生产企业为浙江博锐生物制药有限公司(以下简称“博锐生物”)下属子公司海正生物制药有限公司。2019年12月,贝伐珠单抗注射液(MIL60)III临床研究达到主要研究终点。该项目是比较MIL60和安维汀联合紫杉醇和卡铂治疗晚期或复发性非鳞状非小细胞肺癌(NSCLC)初治受试者的有效性和安全性的随机、双盲、多中心III期研究,由中国医学科学院肿瘤医院王洁教授牵头,全国50家研究中心参与。2020年6月,MIL60上市许可申请获得国家药品监督管理局受理。2021年9月,MIL60 III期临床研究成果亮相2021年欧洲肿瘤内科学会(ESMO)年会。
贝达药业董事长兼首席执行官丁列明博士表示,贝安汀®遵循生物类似药严谨的研发途径,不仅通过了全面的质量相似性研究、非临床相似性研究,而且在在PK特征、临床有效性、安全性和免疫原性等方面表现出与安维汀®高度的相似性。贝安汀®以高品质、高可及性的特点,为转移性结直肠癌和晚期、转移性或复发性非小细胞肺癌患者提供了与原研药物等效优质的治疗选择。
贝达药业副总裁马勇斌表示,贝安汀®是贝达药业第三个获批上市的药物,是公司首个按药品上市许可持有人(MAH)制度申报的品种,也是首个获批的大分子生物制品,它的成功上市标志着贝达药业向大分子抗癌领域迈进了一大步,进一步丰富了公司产品管线。
北京天广实生物技术股份有限公司董事长、总经理李锋博士表示:“非常欣喜看到贝达药业和天广实生物共同开发的贝安汀®在中国成功获批上市。贝安汀®在药学、临床前、和I期临床研究中均显示与贝伐珠单抗高度类似,III期临床结果进一步确证国产抗体类似物与进口原研药疗效一致,期待它为肿瘤患者带来更多选择,让更多患者获得更长生存和更好的生活质量。”
博锐生物总裁王海彬博士表示,很高兴贝安汀®获批上市,为患者提供新的治疗选择。未来博锐生物将深化与贝达药业的合作,共同研制出更多放心好药,惠及更多患者,共同助力健康中国建设。