JAK抑制剂新突破!艾伯维乌帕替尼欧盟获批治疗特应性皮炎(湿疹)
2021年8月24日,艾伯维(AbbVie)宣布,欧盟委员会(EC)批准其口服JAK抑制剂Rinvoq (upadacitinib,乌帕替尼)扩展适应症,用于治疗适合接受全身性治疗的成人和12岁以上青少年中/重度特应性皮炎患者,可选择是否与外用皮质类固醇(TCS)联用。新闻稿指出,乌帕替尼是第1款获批治疗特应性皮炎的JAK抑制剂。
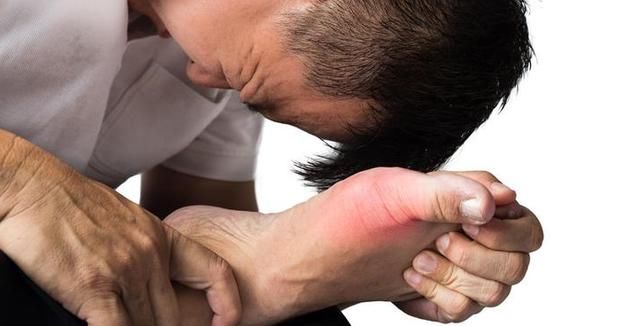
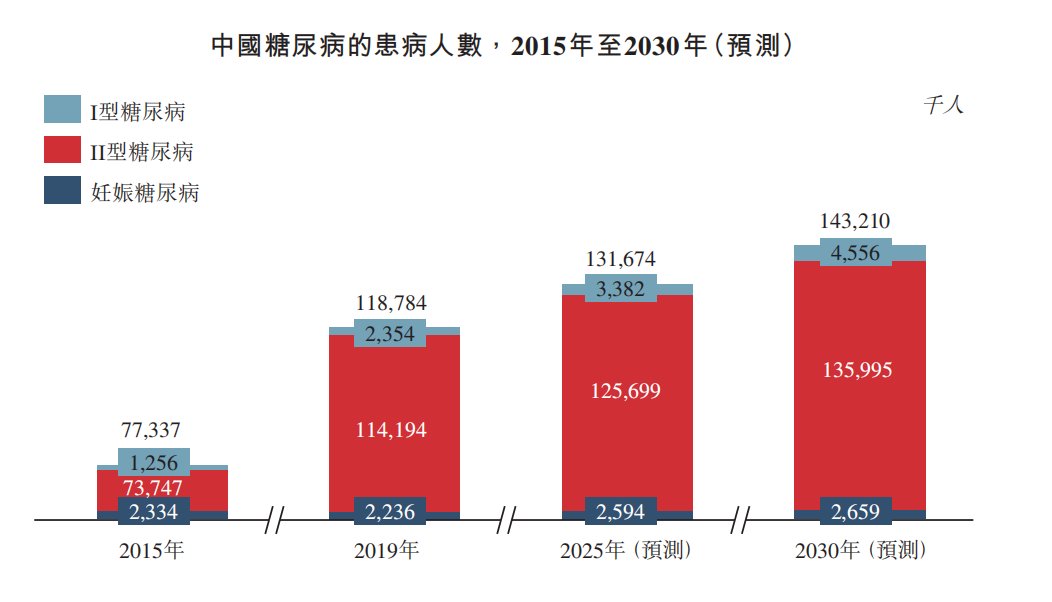
特应性皮炎(AD)是一种常见的、慢性、复发性、发炎性皮肤病,表现为瘙痒和抓挠的反复循环,导致皮肤开裂、鳞片状、渗液。据估计,多达25%的儿童和10%的成人在一生中的某个时候会受到AD影响。20%-46%的成人AD患者会有中度至重度疾病。该病的疾病症状会对患者造成重大的生理、心理和经济负担。
乌帕替尼是一种口服、每日一次的、选择性、可逆性JAK抑制剂。此前,乌帕替尼已在欧盟获批3个适应症:(1)用于治疗对一种或多种疾病修饰抗风湿药物(DMARD)应答不足或不耐受的中度至重度类风湿性关节炎(RA)成人患者;(2)用于治疗对一种或多种DMARD应答不足或不耐受的活动性银屑病关节炎(PsA)成人患者;(3)用于治疗对常规疗法应答不足的活动性强直性脊柱炎(AS)成人患者。本次获批第4个适应症:(4)用于治疗适合接受全身性治疗的成人和12岁以上青少年中/重度特应性皮炎患者,可选择是否与外用皮质类固醇(TCS)联用。在美国,乌帕替尼已被批准用于治疗对甲氨蝶呤(MTX)应答不足或不耐受的中度至重度活动性类风湿性关节炎(RA)成人患者。
在多项3期临床试验中乌帕替尼达到所有主要与次要终点。与安慰剂相比,无论作为单药治疗或与TCS联用,乌帕替尼组患者的皮肤清除和瘙痒缓解程度表现出快速且显著的改善(p<0.001)。
3期试验项目共入组超过2500例中/重度特应性皮炎成人和青少年患者,评估了乌帕替尼单药治疗或与TCS联用,与安慰剂相比的疗效和安全性。15 mg和30 mg剂量的乌帕替尼均达到了所有主要和次要终点。在第16周时,与安慰剂组相比,乌帕替尼组达到湿疹面积和严重程度指数改善75%(EASI 75)和皮肤症状清除/几乎清除(vIGA-AD 0/1)的患者显著更多。并且,乌帕替尼组达到具有临床意义瘙痒减轻(NRS改善≥4)的患者也明显高于安慰剂组。
安全性上,15 mg或30 mg乌帕替尼组最常报告的不良反应(≥5%)为上呼吸道感染(25.4%)、痤疮(15.1%)、单纯疱疹(8.4%)、头痛(6.3%)和血肌酸磷酸激酶(CPK;5.5%)升高。最常见的严重不良反应为严重感染(<1.0%)。该药还有来自各种临床项目中10500例受试者提供的安全性数据支持。
此外,Rinvoq治疗溃疡性结肠炎(UC)、类风湿性关节炎(RA)、银屑病关节炎(PsA)、中轴型脊柱关节炎(axSpA)、克罗恩病(CD)、特应性皮炎(AD)、巨细胞动脉炎(GCA)的III期临床研究正在进行中。